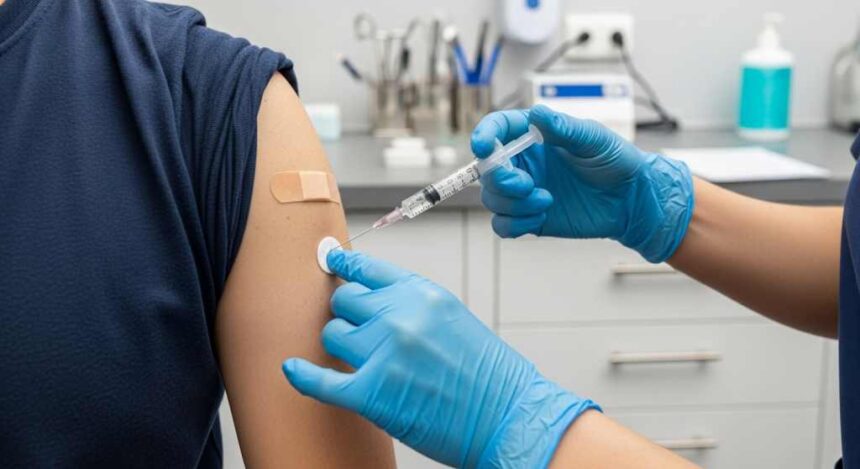
A Fundação Oswaldo Cruz (Fiocruz) vai coordenar um estudo nacional para avaliar uma nova estratégia de prevenção baseada em injeção contra HIV, que exige apenas duas aplicações por ano. A pesquisa pretende analisar a eficácia, a segurança e a viabilidade do uso do medicamento lenacapavir como profilaxia pré-exposição, com foco em populações mais vulneráveis ao vírus, podendo subsidiar uma futura incorporação da tecnologia ao Sistema Único de Saúde (SUS).
Estudo nacional sobre a injeção contra HIV
O projeto, denominado ImPrEP LEN Brasil, será desenvolvido em sete municípios: Campinas, Florianópolis, Manaus, Nova Iguaçu, Rio de Janeiro, Salvador e São Paulo. A iniciativa acompanha a utilização do lenacapavir como método preventivo para pessoas que ainda não vivem com HIV, mas apresentam maior risco de exposição.
A coordenação do estudo ficará a cargo da Fiocruz, que já atua em outras pesquisas relacionadas à profilaxia pré-exposição no país. A proposta é observar, em ambiente real, como a nova injeção contra HIV se comporta em termos de adesão, segurança clínica e potencial de proteção ao longo do tempo.
Medicamento aprovado e formato injetável
O lenacapavir recebeu autorização da Agência Nacional de Vigilância Sanitária (Anvisa) em 12 de janeiro, passando a integrar o conjunto de medicamentos aprovados no Brasil. No contexto do estudo, ele será utilizado exclusivamente na forma injetável, com aplicações realizadas a cada seis meses.
Diferentemente das opções de PrEP atualmente disponíveis, que exigem o uso diário de comprimidos, a aplicação semestral surge como uma alternativa para facilitar a continuidade do método preventivo, especialmente entre pessoas que enfrentam dificuldades para manter o uso regular de medicamentos orais.
O medicamento pertence a uma classe considerada inovadora de antirretrovirais. Sua ação ocorre em diferentes fases do ciclo de replicação do HIV, o que amplia o potencial de impedir que o vírus se estabeleça no organismo. Essa característica sustenta o interesse científico em avaliar seu uso preventivo em larga escala.
Público-alvo e critérios de participação
Para ingressar no estudo, será exigido teste negativo para HIV antes do início das aplicações. A pesquisa é direcionada a homens gays e bissexuais, pessoas não binárias designadas biologicamente do sexo masculino e pessoas transgênero, com idades entre 16 e 30 anos.
As doses utilizadas serão fornecidas pela farmacêutica Gilead Sciences, responsável pelo desenvolvimento do medicamento. O início efetivo das aplicações depende da chegada ao país de agulhas específicas necessárias para a administração correta do lenacapavir.
Caminho até o SUS
Além de analisar os resultados clínicos, os dados coletados deverão contribuir para as etapas regulatórias que antecedem uma eventual oferta pelo SUS. Antes disso, o medicamento ainda passará pela definição de preço máximo pela Câmara de Regulação do Mercado de Medicamentos (CMED).
Na sequência, a Comissão Nacional de Incorporação de Tecnologias no SUS (Conitec) avaliará as evidências científicas produzidas, emitindo um parecer técnico ao Ministério da Saúde sobre a viabilidade da adoção da nova tecnologia.